À travers l'événement annuel de recrutement, l'ICG offre aux meilleurs candidats une occasion unique de visiter l'institut, de rencontrer les étudiants et les professeurs actuels, et de découvrir les opportunités de recherche de pointe. Les participants sélectionnés peuvent également recevoir une bourse d'admission, avec les frais de voyage pris en charge pour ceux qui sont invités.
Les candidatures
pour 2025
sont désormais ouvertes
Les meilleurs candidats seront invités à assister à l'événement qui vise à être à la fois informatif et convivial. Nous présenterons le vaste programme de formation de l'ICG et offrirons l'opportunité de rencontrer des étudiants diplômés existants et des scientifiques en oncologie. Les candidats sélectionnés seront ensuite offerts une bourse pour l'admission à l'automne 2025 ou à l'hiver 2026. Veuillez noter que tous les frais de déplacement seront couverts pour les étudiants invités, sauf indication contraire.
Participez à notre séance d'information en direct pour poser vos questions et en apprendre davantage sur le programme le 19 novembre à 16 h (heure de l'Est). La séance d'information se déroulera en anglais, avec une période de questions en français et en anglais.
Les candidats intéressés doivent remplir un formulaire d'inscription en ligne ici.
Dans le formulaire d'inscription en ligne, les candidats devront télécharger les informations suivantes dans un seul fichier PDF :
- Un CV à jour avec des informations de contact valides
- Une lettre de motivation (maximum 2 pages)
- Une copie de vos relevés de notes les plus récents (ces documents n'ont pas besoin d'être officiels pour cet événement)
L'inscription est ouverte
Date limite de soumission des candidatures
1er décembre 2024
Événements en personne
23 - 24 janvier 2025
- Intérêt démontré pour la recherche biomédicale
- Inscription dans un programme de B.Sc. ou de M.Sc.
- Moyenne cumulative de 3,6 sur 4,3 pour les candidats M.Sc. et Ph.D. ; les étudiants internationaux seront évalués individuellement.
L'ICG s'engage en faveur de l'équité et de la diversité dans le recrutement de ses étudiants. Nous encourageons les candidatures des personnes racialisées/minorités visibles, des femmes, des personnes autochtones, des personnes en situation de handicap, des minorités ethniques, des personnes de minorités sexuelles et de genres, ainsi que d'autres personnes susceptibles de contribuer à la diversification.
Les chercheurs suivants recrutent actuellement de nouveaux étudiant.e.s :
Les inhibiteurs de points de contrôle immunitaire ont révolutionné le traitement du cancer. Ceux-ci permettent aux cellules immunitaires, particulièrement les lymphocytes cytotoxiques, de détruire les cellules cancéreuses. Cependant, de nombreux patients ne démontre aucun bénéfice suite à ces immunothérapies. Nous avons découvert que la production d’adénosine par l’axe CD39-CD73 constitue un point de contrôle immunitaire majeur qui favorise le cancer. Avec le soutien des Instituts de recherche en santé du Canada, nous définissons l’écosystème moléculaire qui gouverne les effets médiés par l’adénosine dans le cancer. Plus précisément, nous étudions l’impact des enzymes CD39 et CD73 ainsi que l’impact des transporteurs de l’adénosine ENT1 et ENT2 dans la réponse immunitaire anti-tumorale.
Nous exploitons également de vastes ensembles de données multi-omiques afin d’identifier de nouveaux mécanismes de résistance à l’immunothérapie. Nous travaillons en étroite collaboration avec les chercheurs du réseau Marathon de l’Espoir de l’Institut Terry Fox, l’Institut Francis Crick et les Centres d’excellence en recherche sur l’immunothérapie de Roche (imCORE). Notre consortium nous permet d’explorer, à un niveau sans précédent, les associations génomiques, transcriptomiques et protéomiques avec les réponses cliniques à l’immunothérapie.
Recherche
en cours
Avec des partenaires en Belgique, en France et en Allemagne, et avec notre collaboratrice de l'ICG, la Dr Morag Park, nous cartographions l'adaptation du cancer du sein triple négatif à la chimio-immunothérapie. Ce projet s'appuie sur la transcriptomique spatiale et l'analyse multiplexe des lésions primaires et métastatiques issues de trois grands essais cliniques randomisés.
Nous avons récemment découvert que le blocage ou la suppression de l'ENT1, principal régulateur des concentrations d'adénosine extracellulaire, renforçait considérablement l'immunité antitumorale dépendante des lymphocytes T CD8+. À l'aide de souris génétiquement modifiées et de modèles précliniques de cancer, nous caractérisons actuellement la fonction spécifique des ENT1 et ENT2 dans diverses populations de cellules immunitaires.
Grâce à la bio-informatique, nous avons découvert que le récepteur 2 activé par les protéases (PAR2) pourrait constituer une nouvelle cible potentielle pour surmonter la résistance aux inhibiteurs de points de contrôle immunitaires. Le PAR2 est un récepteur activé par des protéases tumorales spécifiques et impliqué dans l'inflammation physiopathologique. Nous étudions l'impact du PAR2 sur l'immunité tumorale à l'aide de souris génétiquement modifiées et d'analyses protéomiques de tumeurs humaines, et nous identifierons les populations de patients susceptibles de bénéficier d'un traitement ciblant le PAR2.
En collaboration avec le CHUM et l'Institut de recherche de l'Hôpital d'Ottawa, nous définissons le paysage immunitaire et les interactions fonctionnelles au niveau unicellulaire des cancers ovariens rares. Notre objectif est d'identifier de nouveaux biomarqueurs pour le diagnostic et de nouvelles trajectoires de traitement, notamment des immunothérapies et des conjugués anticorps-médicaments.
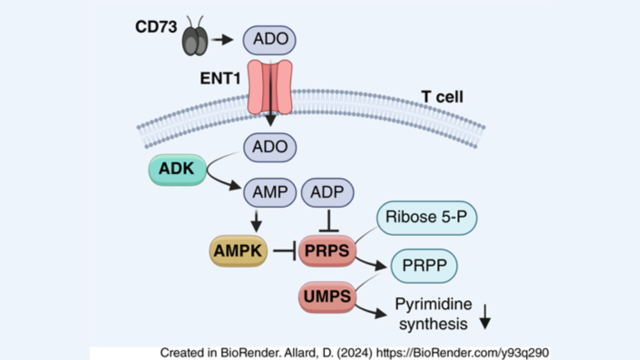
- ENT1 : une nouvelle cible thérapeutique Nous avons étudié l’effet du transporteur équilibratif de nucléosides-1 (ENT1), principal régulateur des concentrations extracellulaires d’adénosine, sur l’immunité antitumorale. Le blocage ou la délétion d’ENT1 chez l’hôte a significativement renforcé les réponses antitumorales dépendantes des lymphocytes T CD8+. Les tumeurs greffées chez des souris déficientes en ENT1 présentaient une infiltration accrue de lymphocytes T CD8+ effecteurs, dotés d’un profil transcriptomique cytotoxique renforcé. Sur le plan mécanistique, la captation d’adénosine médiée par ENT1 inhibait l’activité de la phosphoribosyl-pyrophosphate synthétase dans les lymphocytes T activés, supprimant ainsi la production d’uridine-5′-monophosphate et de ses dérivés nécessaires à la synthèse de l’ADN et de l’ARN. ENT1 as a new Target We investigated the effect on tumor immunity of equilibrative nucleoside transporter-1 (ENT1), the major regulator of extracellular adenosine concentrations. Blocking or deleting host ENT1 significantly enhanced CD8+ T-cell–dependent antitumor responses. Tumors inoculated into ENT1-deficient mice showed increased infiltration of effector CD8+ T cells with an enhanced cytotoxic transcriptomic profile. Mechanistically, ENT1-mediated adenosine uptake inhibited the activity of phosphoribosyl pyrophosphate synthetase in activated T cells, thereby suppressing production of adenosine receptors suppress immune cells. uridine 5′-monophosphate and its derivatives required for DNA and RNA synthesis.
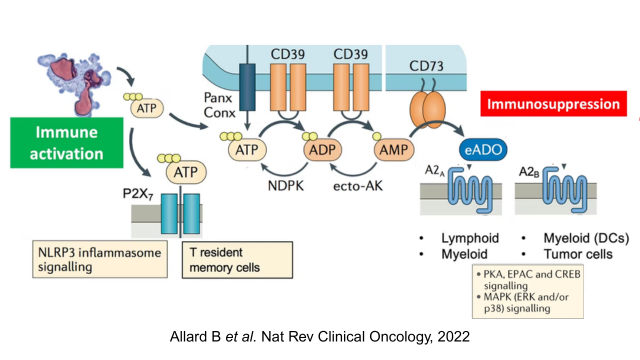
- Voie de l'adénosine On sait depuis près d'un demi-siècle que l'adénosine (ADO) module la fonction immunitaire. Les niveaux d'ADO extracellulaire sont contrôlés par l'hydrolyse de l'adénosine triphosphate extracellulaire par des ecto-nucléotidases telles que CD39 et CD73. La signalisation de l'adénosine nuit à la fonction de diverses cellules immunitaires, y compris les cellules T, les cellules NK et les cellules myéloïdes. L'activation de la PKA dépendante de l'AMPc et le blocage des voies NF-KB et JAK-STAT sont des mécanismes généralisés par lesquels les récepteurs A2A et A2B de l'adénosine suppriment les cellules immunitaires. The Adenosine pathway Adenosine (ADO) has been known to modulate immune function for nearly half a century. Levels of extracellular ADO are controlled by the hydrolysis of extracellular adenosine triphosphate by ecto-nucleotidases such as CD39 and CD73. Adenosine signaling impairs the function of a variety of immune cells, including T cells, NK cells and myeloid cells. Activation of cAMP-dependent PKA and blockade of NF-KB and JAK-STAT pathways are generalized mechanisms by which A2A and A2B adenosine receptors suppress immune cells.
- Professeur, Institut du cancer Rosalind et Morris Goodman, McGill University, Faculté de Médicine, Département de Microbiologie et Immunologie
- Professeur associé, Faculté de pharmacie, Université de Montréal
Équipe
Découvertes majeures
- 2025 Adenosine Uptake through the Nucleoside Transporter ENT1 Suppresses Antitumor Immunity and T-cell Pyrimidine Synthesis
- 2025 The Terry Fox Research Institute Marathon of Hope Cancer Centres Network: A pan-Canadian precision oncology initiative
- 2025 Targeting G Protein-Coupled Receptors in Immuno-Oncological Therapies
- 2023 CD73 Inhibits cGAS–STING and Cooperates with CD39 to Promote Pancreatic Cancer
- 2023 Adenosine A2A receptor is a tumor suppressor of NASH-associated hepatocellular carcinoma
- 2022 Leveraging big data of immune checkpoint blockade response identifies novel potential targets






.png)
.png)
.png)